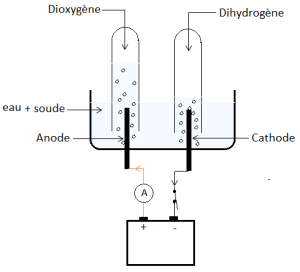
Observations
Méthode :
Méthode : Identification du gaz recueilli à la cathode
Le gaz recueilli à la cathode s'enflamme en émettant un bruit caractéristique (on dit qu'il aboie) et brûle avec une flamme pâle: il s'agit du dihydrogène.
La vidéo ci-dessous montre comment identifier le dihydrogène (dans la vidéo, le dihydrogène est obtenu par une autre réaction que l'électrolyse de l'eau).
Méthode : Identification du gaz recueilli à l'anode
Le gaz recueilli à l'anode rallume une bûchette ne présentant plus qu'un point incandescent : il s'agit du dioxygène, gaz qui entretient les combustions.
La vidéo ci-dessous montre comment identifier le dioxygène.
Méthode : Interprétation
La formation de dihydrogène et de dioxygène aux électrodes montre qu'il y a apparition de nouveaux corps et que des réactions chimiques se produisent.
La déviation de l'aiguille de l'ampèremètre (ou l'éclairement de la lampe) montre qu'un courant électrique traverse le circuit.
Le dihydrogène et le dioxygène n'apparaissent que quand le courant électrique traverse le circuit: les gaz formés sont le résultat d'une électrolyse.
À la fin de l'électrolyse la quantité d'ions apportés par la soude n'a pas varié: l'électrolyse se résume donc à la décomposition de l'eau.
Fondamental : Conclusion
Le passage du courant électrique dans de l'eau additionnée de soude décompose l'eau en dihydrogène et en dioxygène dans les proportions d'un volume de dioxygène et de deux volumes de dihydrogène.
Complément : L'électrolyse de l'eau
La vidéo ci-dessous montre les différentes étapes de l'expérience de l'électrolyse de l'eau. L'électrolyte utilisé dans cette expérience n'est pas de l'eau additionnée de soude, mais de l'eau additionnée d'acide sulfurique. Les résultats sont exactement les mêmes.