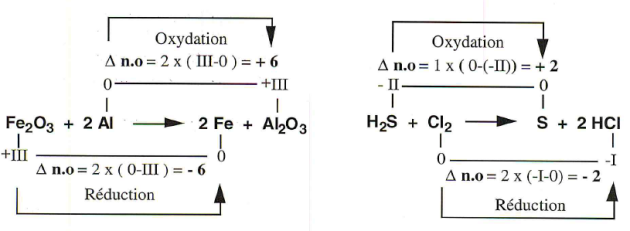
Utilisation du nombre d'oxydation
Définition : Définition
Il y a oxydation d'un élément si son nombre d'oxydation (n.o) augmente.
Il y a réduction d'un élément si son nombre d'oxydation (n.o) diminue.
Attention :
Si au cours d'une réaction chimique ; les nombres d'oxydation des éléments ne varient pas, alors cette réaction n'est pas une réaction d'oxydoréduction.
Utilisation du nombre d'oxydation pour équilibrer quelques réactions d'oxydoréduction
Au cours d'une réaction d'oxydoréduction, la somme de tous les nombres d'oxydation gagnés est égale à la somme de tous les nombres d'oxydation perdus.
On dit que :